
Je me demande comment nos recherches se termineront,
car il semble que le sujet du saumon OGM ait plutôt bien marché pour les Habrachiters. Pendant que nous préparons du matériel sur la modification des plantes, je suggère d'examiner un sujet tout aussi intéressant - la modification génétique de l'Homo Sapiens. C'est un sujet très controversé et holivar, qu'il est inutile d'ignorer.
Je vais tout de suite donner plusieurs thèses qui peuvent sembler controversées, mais qui doivent en quelque sorte être résolues dans la communauté scientifique:
- Nous dégénérons. Chaque année, des individus plus faibles survivent, donnant naissance à des enfants et alourdissant le pool génétique. Il doit être corrigé.
- De simples interdictions n'aideront pas. Si les expériences sont interdites en Europe, alors, par exemple, la Chine les réalisera.
- Nous ne nous arrêterons pas au traitement des maladies génétiques. Tôt ou tard, les militaires se joindront à leurs super-soldats et à ceux qui veulent des enfants plus forts et plus intelligents aux yeux bleus.
Je vais essayer de donner un aperçu des techniques d'intervention existantes dans le génotype des personnes et en même temps nous analyserons de quoi il nous menace.
Qu'est-ce que la thérapie génique
Définissons d'abord la terminologie. La thérapie génique est une intervention sur le génome humain dans le but de traiter certaines maladies. De plus, l'intervention ne concerne que les cellules somatiques. Ce sont les cellules qui ne se reproduisent pas. Nous n'avons clairement pas besoin de corriger les mutations et les corrections de bogues dans les nouvelles générations. Pour l'instant, du moins.
De véritables expériences sur les animaux ont commencé vers les années 1980, mais il ne s'agissait alors que d'étapes timides. Nous n'avions aucune beauté comme les imprimantes à ADN, exprimant des vecteurs pour les eucaryotes.
Où pouvons-nous vraiment intervenir?
Les plasmides
Pour commencer, vous pouvez quitter le noyau cellulaire, qui contient les informations génétiques de base. Vous pouvez utiliser des plasmides.

1) ADN chromosomique de bactéries 2) Plasmides
Les plasmides sont presque exclusivement bactériens. Parfois trouvé dans les champignons primitifs et certaines plantes. En fait, c'est de l'ADN, mais plié en un anneau et flottant séparément dans le cytoplasme. Autrement dit, un tel mécanisme séparé pour stocker le matériel génétique. Pour les bactéries, ils sont très importants pour transmettre des mutations positives, par exemple pour «informer les voisins» des options de protection antibiotique. L'astuce des plasmides lorsqu'ils sont utilisés chez l'homme est qu'ils se désagrègent d'eux-mêmes après un certain temps après avoir été introduits dans la cellule. Et ils n'affectent pas non plus le principal appareil génétique de la cellule. Autrement dit, le micrologiciel principal ne sera pas affecté.
Patcher le noyau
Ensuite, nous avons la possibilité de modifier directement l'extrait de code dans le noyau. Il s'agit d'une procédure plus invasive et comporte déjà le risque d'insérer ou de découper incorrectement un morceau d'ADN. Mais c'est pratiquement la seule option pour corriger radicalement un défaut génétique grave, car les cellules somatiques vont se diviser et transmettre la version corrigée de l'ADN à leurs descendants.
Mitochondries
Les mitochondries sont comme des réacteurs nucléaires dans une cellule. Ils consomment des acides gras et du glucose, et à la sortie ils tamponnent les macroergs - des substances à haute énergie de liaison. Par exemple, ATP. C'est un «carburant» universel pour toutes les réactions actives, par exemple pour le fonctionnement de pompes à membrane osmotique contre un gradient de concentration.
Ils ont une particularité - leur propre appareil génétique. En fait, ils ressemblent à des symbiotes semi-autonomes pour cette raison même. Leur appareil génétique a du sens pour régner avec des mutations congénitales dans l'ADN mitochondrial. Il s'agit généralement de syndromes congénitaux très graves.
Le vecteur viral est comme une seringue
Le premier point clé est le développement d'outils de livraison - des vecteurs viraux. Le premier virus de ce type pour les mammifères a été développé en 1984. Un rétrovirus murin a été utilisé comme seringue moléculaire. Il était en soi un outil très désagréable, car avec une forte probabilité, il provoquait des maladies oncologiques. En fait, son deuxième nom est le virus de la leucémie murine (MLV). À l'avenir, le développement est passé à des options plus sûres.
Qu'est-ce qu'un vecteur viral exactement? Il s'agit d'un virus spécialement modifié qui ne fonctionne qu'une seule fois. Comme une seringue. Pour ce faire, il doit répondre à plusieurs critères:
Sécurité
Le vecteur viral ne doit pas pouvoir se multiplier spontanément. Pour cela, ils ont un kill-switch intégré. Leur génome est initialement tellement endommagé qu'ils ne peuvent pas se reproduire de manière autonome. Dans un environnement de laboratoire, ils se multiplient en culture cellulaire uniquement en présence de composants irremplaçables et de virus auxiliaires supplémentaires qui produisent une partie des protéines nécessaires à l'assemblage. Autrement dit, il se multiplie dans un flacon de culture de laboratoire, mais dans le corps, il agit une fois, quitte la cellule sous une forme semi-assemblée et meurt.
Faible cytotoxicité
De nombreux virus sont très cruels envers les cellules hôtes. Après la phase d'incubation, la cellule meurt d'épuisement et de nouveaux virions se dispersent de sa dépouille mortelle dans toutes les directions. Dans le même temps, il existe des virus qui n'affectent pas particulièrement la physiologie normale des cellules sur lesquelles ils parasitent. Par exemple, les adénovirus.
Stabilité
Les virus doivent être génétiquement stables. Par exemple, la grippe ne fonctionnera pas. Il n'a pas de mécanismes intelligibles de "parité" et il se fiche que le hachage après copie n'ait pas convergé. C'est sa stratégie évolutive. Les mêmes coronavirus, au contraire, ont des mécanismes de contrôle et de réparation, ce qui donne une plus grande stabilité du matériel génétique. Bien qu'ils ne soient pas utilisés comme vecteur pour d'autres raisons. Ainsi, la tâche est de s'assurer que le virus en cours de reproduction dans des bioréacteurs conserve la même charge utile - la charge utile inchangée.
Spécificité du type de cellule
Le virus doit livrer sa charge non seulement n'importe où, mais exactement dans un type spécifique de cellules. Cela signifie que si nous devons guérir une maladie associée à des érythrocytes défectueux, le virus doit alors infecter très précisément les cellules souches précurseurs multipotentes des cellules sanguines. Et en même temps, n'accrochez pas, par exemple, le tissu musculaire.
Ce qui se fait déjà en matière de thérapie génique
La première correction génétique humaine a été effectuée en 1990. Ashanti DeSilva, 4 ans, a reçu un traitement pour un défaut génétique sévère d'immunodéficience combinée complexe associée à une carence en enzyme ADA. Il convient de noter que ce n'est pas le génome des cellules souches qui produisent les lymphocytes T qui ont été édités, mais les cellules T adultes du sang de son propre donneur. Autrement dit, elle devait répéter ces procédures à l'avenir. Ensuite, il y avait une série de protocoles expérimentaux réussis pour le traitement du SCID (déficit immunitaire combiné sévère) en utilisant une technique similaire.
En 1999, un incident s'est produit qui a considérablement ralenti les recherches dans ce domaine. Jesse Gelsinger, souffrait d'une maladie génétique du foie en raison de laquelle elle était incapable de détoxifier l'ammoniac. 4 jours après l'introduction d'un vecteur adénoviral avec une copie saine du gène, il est décédé des suites d'une réponse hyperimmunisée et d'une défaillance d'organes multiples. Par la suite, la FDA a conclu qu'il y avait de nombreuses violations dans le protocole d'étude.
En 2006, les premiers rapports de protocoles de thérapie génique individuelle réussis pour le traitement de l'oncologie sont apparus. Les cellules T tueuses sont programmées pour un type spécifique de tumeur, puis libérées dans le corps du patient. Thérapie anti-VIH reconnue
en 2011 chez le patient Gero Hütter en 2008. La méthode n'est pas particulièrement applicable à un large public, car elle nécessite l'ablation complète de sa moelle osseuse, puis l'implantation de cellules corrigées avec une double mutation delta-32 qui désactive le récepteur CCR5.
En 2013, il n'y avait que cinq médicaments géniques autorisés dans le monde. Trois en oncologie, glybera pour le traitement du déficit héréditaire en lipoprotéine lipase et néovasculgen. Ce dernier, d'ailleurs, a été complètement développé par nous.
Néovasculgen
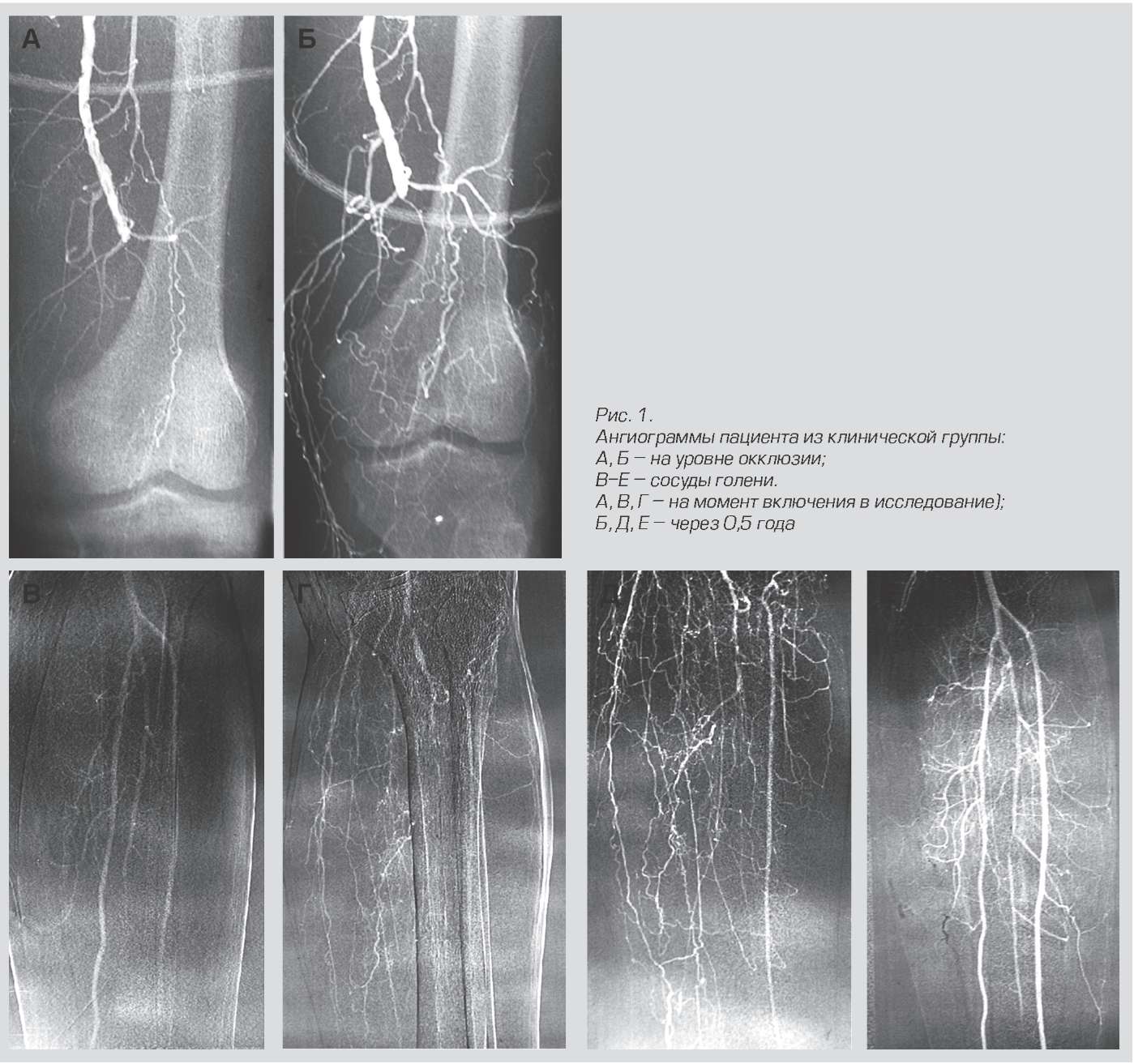
Résultats du traitement avec Neovasculgen.
Ce médicament appartient au plasmide, c'est-à-dire qu'il n'édite pas son propre génome de la cellule, mais ne lui délivre que des plasmides qui fonctionnent pendant un temps limité.
(), VEGF 165, (VEGF — Vascular Endothelial Growth Factor). , . , , .
Human Stem Cell Institute
Le mécanisme d'action est intéressant. Les cellules au site d'injection commencent à synthétiser le VEGF, un facteur de croissance vasculaire. En conséquence, un nouveau réseau capillaire ramifié commence à se développer dans cette zone. Ceci est essentiel pour les patients atteints d'ischémie chronique des membres inférieurs due au diabète et à l'athérosclérose, par exemple. Avant ce médicament, il y avait plus d'amputations. Maintenant, il a également été testé pour une utilisation en dentisterie pour la greffe d'implants. La préparation du gène est mélangée avec du matériel osseux et suturée. En conséquence, les vaisseaux se développent rapidement et le tissu nécessaire se forme sans rejet. Les lapins ont déjà été simulés avec précision lors de la transplantation de fragments de crâne. Les gens sont les suivants, pour autant que je sache.
Zolgensma
L'atrophie musculaire spinale est une maladie très grave, cliniquement quelque peu similaire à la sclérose latérale amyotrophique dont Hawking a souffert, mais a d'autres causes. À la suite du développement de la maladie, la paralysie progresse, ce qui se termine par la mort en raison de l'incapacité de respirer.
Zolgensma est le premier médicament de thérapie génique pour l'atrophie musculaire spinale. Produit par AveXis (Novartis). Une copie de travail du gène SMN est injectée en utilisant le sérotype 9 du virus adéno-associé (AAV), AAV9, qui est capable de traverser la barrière hémato-encéphalique et de pénétrer dans les cellules du patient. Un problème - cela coûte de l'argent absolument monstrueux. Une injection coûte plus de 2,1 millions de dollars (environ 152 millions de roubles). Mais les résultats sont également étonnants. Chez l'homme, la fonction motrice est restaurée et la maladie ne progresse pas davantage. En théorie, ces manipulations coûteuses devraient être payées par l'État. Pour les particuliers, le coût du traitement des maladies rares est tout simplement prohibitif.
Et après?
Voici une question très difficile. Nous accumulons des gènes défectueux dans la population. Auparavant, un enfant souffrant d'une malformation cardiaque mourrait tout simplement - maintenant ils le sauveront et il donnera une progéniture avec ce défaut. Auparavant, de nombreuses grossesses ne duraient pas - maintenant, les femmes enceintes sont retirées avec un pourcentage minimum de fausses couches et se terminent par des naissances réussies. En fait, nous brisons les mécanismes d'abattage naturel de la population. C'est correct et humain, mais il faut faire quelque chose avec les mutations qui s'accumulent dans le pool génétique.
Soit nous arriverons aux cartes vertes et aux permis de reproduction, soit nous apprendrons à corriger de manière fiable et sûre les anomalies génétiques. Ce serait cool de jeter la myopie, la dysplasie systémique du tissu conjonctif et un tas d'autres malformations congénitales. Et enfin, corrigez ce gène cassé stupide responsable de la synthèse de la vitamine C à partir du glucose, comme tous les mammifères normaux.
Ici, seul un avenir inconnu nous attend plus loin. Le plus alarmant est la stratification potentielle de la société, lorsque les segments les plus riches de la population modifient leurs enfants pour qu'ils soient exempts de diabète, d'athérosclérose et en même temps écrasent un peu de myostatine pour les rendre sportifs sans trop d'effort. Frais. Mais ça fait peur.
