
Pour la première fois, les biologistes américains ont forcé les neurones rétiniens endommagés par le glaucome à se régénérer . La réalisation a eu lieu en partie grâce à une «reprogrammation» biologique. Des vecteurs viraux avec des gènes de facteurs Yamanaka ont été injectés dans les yeux de souris aux yeux blessés. En conséquence, les neurones ont retrouvé leur efficacité. Un résultat similaire a été obtenu chez les rongeurs âgés.
Le vieillissement est un processus irréversible, il conduit d'abord à un dysfonctionnement des tissus, puis à leur mort. Avec le temps, notre système nerveux central perd sa capacité à récupérer, en même temps, le nombre de cellules souches dans le corps humain diminue.
Une zone spécifique du globe oculaire, qui contient des bâtonnets, des cônes, ainsi que des neurones et des synapses, est la rétine. Il est situé à l'intérieur de l'arrière du globe oculaire. Ses neurones et synapses transmettent des informations lumineuses des yeux à notre cerveau. Les dommages à la rétine entraînent une perte de vision. Auparavant, on pensait que ce tissu n'était pas capable de récupérer. Il s'avère que tout n'est pas si simple, il y a de l'espoir.
Contrôle des cellules
Pour comprendre comment des scientifiques de la Harvard Medical School ont réussi à forcer la rétine à se rétablir, examinons le concept d '«âge biologique».
Les cellules anciennes et nouvelles contiennent de nombreux marqueurs épigénétiques - des marqueurs méthyliques sur les protéines ADN et histones . L'ensemble des étiquettes ADN peut être utilisé pour mesurer l'âge biologique, également appelé horloge épigénétique .
Si les scientifiques savaient comment réduire l'âge biologique des cellules, ils auraient en fait inventé l'immortalité. Il n'y a pas encore de telles déclarations choquantes. Mais il y a quelques années, la méthode de «remise à zéro» de l'âge épigénétique est devenue connue. Il a été découvert par le scientifique japonais Shinya Yamanaka (山 中 伸 弥), pour lequel il a reçuPrix Nobel. La méthode consiste en ce que 4 facteurs Yamanaki (du nom du scientifique) ou facteurs de transcription sont introduits dans les cellules. Grâce à cette procédure, les cellules deviennent des cellules souches, similaires aux cellules aux premiers stades de l'embryogenèse. Avec les cellules, l'âge est également réinitialisé. Cette méthode révolutionnaire ne peut pas être appliquée à tout le corps humain ou à de grandes masses de tissus. Cependant, il peut être utilisé localement et pendant une durée déterminée, provoquant une reprogrammation contrôlée des cellules. Cette procédure a longtemps été testée sur des souris modifiées.
Dans le cas de la vision, les scientifiques américains se sont également tournés vers les rongeurs expérimentaux. Les experts ont mis au point un vecteur spécialisé, appelé "adénoviral". Sa tâche est de fournir trois des quatre facteurs Yamanaka aux cellules. Le quatrième a été reconnu comme le plus dangereux, capable de provoquer des tumeurs malignes, ils ont donc décidé de l'abandonner. L'essentiel est que les facteurs soient livrés de manière ciblée et non simplement introduits dans le corps. Les vecteurs ne sont activés que par une substance spéciale - la doxycycline . Les scientifiques peuvent arrêter ou démarrer le travail des facteurs de manière simple - ajoutez cette substance à l'eau potable pour les rongeurs.
Comment s'est déroulée l'expérience?
Dans un premier temps, les scientifiques étaient convaincus de l'innocuité de la méthode pour les souris: ils ont introduit le vecteur à des individus d'âges différents. Ils ont observé comment se comportent les jeunes souris âgées de cinq mois et âgées de vingt mois lorsque le vecteur est activé. Il n'y a eu aucun changement significatif.

À l'étape suivante, les scientifiques ont testé l'action des vecteurs sur les cellules ganglionnaires de la rétine, qui servent de conducteurs de l'influx nerveux des yeux au cerveau. Une caractéristique de ces cellules est la capacité de se régénérer et de développer de nouveaux axones chez les embryons et les nouveau-nés. Ces propriétés se perdent avec l'âge. Par conséquent, avec le glaucome, le nerf optique s'atrophie.
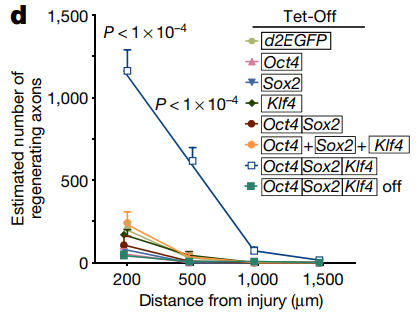
Le nombre d'axones régénérants en fonction de l'action de 1,2 ou 3 facteurs Des
souris Yamanaka ont été injectées avec des vecteurs viraux dans les yeux. Après leur avoir donné de la doxycycline, ils ont commencé l'action. Après cela, le nerf optique a été endommagé. Et puis un colorant a été injecté afin de marquer les axones en croissance . En conséquence, en fonction du nombre de facteurs (1, 2 ou les 3) axones, un nombre différent a augmenté. La combinaison des trois facteurs a donné la croissance maximale. Le résultat a été observé chez les individus jeunes et plus matures. En théorie (in vitro), un résultat similaire serait pour les neurones humains.
De plus, les scientifiques ont été convaincus de l'action de l'approche dans deux cas: avec des lésions du nerf optique à la suite d'un traumatisme et avec une diminution de l'acuité visuelle liée à l'âge.
Chez les souris aux yeux blessés, le glaucome a été artificiellement induit en augmentant la pression oculaire par injection de microbilles. Après cela, les facteurs ont été injectés et activés pendant un mois. Les mesures ont montré qu'au final, il était possible de restaurer environ 50% de la vision perdue.
De manière frappante, dans le cas des souris âgées, l'acuité visuelle est presque revenue à celle des jeunes individus. Les scientifiques pensent qu'en théorie, cela fonctionnera également pour les humains.
Les scientifiques ont déjà fait une déclaration sur la capacité de la rétine à récupéreril y a quelques mois. Ensuite, des chercheurs de l'Université Johns Hopkins ont déclaré que ses tissus pouvaient se régénérer. Ils ont constaté qu'en général, les mammifères ont le potentiel de régénérer des tissus individuels, mais la pression évolutive l'a désactivé. Ils pensent que l'arrêt était dû à une lutte entre la régénération du SNC et la résistance des parasites. Cependant, le processus peut être influencé en activant les bons gènes.
