Pertinence de la formation
Une étape importante dans le développement de la classification de l'ordre des puces est associée au développement de la recherche génomoléculaire. Actuellement, grâce à ces méthodes, la parenté des ordres de puces et de mécoptères est confirmée. Les gènes de l'ADN ribosomal, le facteur d'élongation de la synthèse des protéines et le gène mitochondrial cytochrome oxydase II (COII), qui ont été étudiés chez des représentants de la plupart des familles de l'ordre des mécoptères, ainsi que 128 espèces de 83 genres de puces de 16 familles, sont activement étudiés (S.G. Medvedev. 2009; Whiting 2002; Whiting et al.2008). La phylogénie des puces est reconstruite à partir de données sur ces gènes par diverses méthodes de construction d'arbres phylogénétiques et de modèles de calcul des distances par paires, souvent présentés sous la forme d'un arbre consensus (consensus strick) (Whiting et al.2008). Cependant, dans certains cas, les résultats des études génomoléculaires contredisent le schéma des liens familiaux,obtenu sur la base d'une analyse phylogénétique. En outre, conformément aux différentes interprétations des données de génétique moléculaire, l'origine des infra-commandes clés des puces peut être interprétée de différentes manières. Ainsi, du point de vue de différents auteurs, les mêmes clades de puces peuvent être à la fois des groupes polyphylétiques et monophylétiques (Whiting et al.2008, S.G. Medvedev.2019). Cela peut être dû à la fois aux particularités de l'écologie de la faune aux puces moderne et à divers problèmes méthodologiques liés au travail avec des données génétiques moléculaires.et les groupes monophylétiques (Whiting et al.2008, S.G. Medvedev.2019). Cela peut être dû à la fois aux particularités de l'écologie de la faune aux puces moderne et à divers problèmes méthodologiques liés au travail avec des données de génétique moléculaire.et les groupes monophylétiques (Whiting et al.2008, S.G. Medvedev.2019). Cela peut être dû à la fois aux particularités de l'écologie de la faune aux puces moderne et à divers problèmes méthodologiques liés au travail avec des données génétiques moléculaires.
En ce qui concerne le premier point, il convient de souligner que l'isolement de lignées phylétiques distinctes de puces, qui ont un statut égal en taxonomie, s'est produit à des intervalles historiques différents. Cela signifie à son tour que la faune aux puces est constituée de fragments dispersés d'une vaste paléofaune, qui est maintenant en grande partie éteinte (S.G. Medvedev.2009, S.G. Medvedev.2019). Il en découle qu'avec différentes approches méthodologiques des études moléculaires génétiques, on peut perdre de vue l'évolution convergente des séquences nucléotidiques (homoplasie), qui peut conduire à des erreurs dans la détermination de la topologie de l'arbre et à un faible support statistique des branches. Ainsi, par exemple, en utilisant des données qui ont des relations différentes pour différents taxons et, par conséquent, des relations différentes avec différentes parties de gènes,nous trouverons des lacunes dans les séquences et le manque de données pour différents loci pour différents échantillons (S.G. Medvedev.2019, Lukashov V.V.2006). Par conséquent, lors du choix d'une méthode de recherche, tous ces problèmes doivent être pris en compte et des échantillons des taxons de puces les plus étudiés et les plus courants doivent être sélectionnés afin de les comparer ensuite avec les échantillons de mécoptères les plus étudiés. De cette façon, nous pouvons construire un arbre plus fiable avec un support élevé.
, Siphonaptera Mecoptera -II (COII).
:
Siphonaptera NCBI [5], .
(COX 1) Siphonaptera .
-II (COII) Mecoptera Siphonaptera NCBI [1].
MEGA X.
.
NCBI [5] : Chaetopsylla globiceps (Taschenberg, 1880), Chaetopsylla trichosa (Kohaut, 1903), Ctenocephalides felis (Bouché, 1835), Ctenocephalides canis (Curtis, 1826), Ceratophyllus sciurorum (Schrank, 1803), Leptopsylla segnis (Schönherr, 1811). , NCBI[1], Boreus: Boreus westwoodi (Hagen, 1866), Boreus hymalis (Linnaeus, 1767), Boreus coloradensis (Byers, 1955), Boreus nivoriundus (Fitch, 1847), Boreus brumalis (Fitch, 1847), Boreus californicus (Packard, 1870), (.1.).
UPGMA [2] , - 500 [3]. Muscle (. 2.) MEGA X [4]. Muscle . , . translate DNA to protein and vice versa (.3), . (. 3.) , - , . (.4). MEGA . Modeltest 3.06 PPC (Posada, D., Crandall, K.C., 1999) (AIC), . AIC , , (Posada, D., Buckley, T.R., 2004.). MEGA X [4] 64- Windows 10 Home 4- INTEL 1,6 1 .
- [6] (.5.). 12 . 1-+2-+3-+. ( ). 742 .
( 1.)

(.2.)
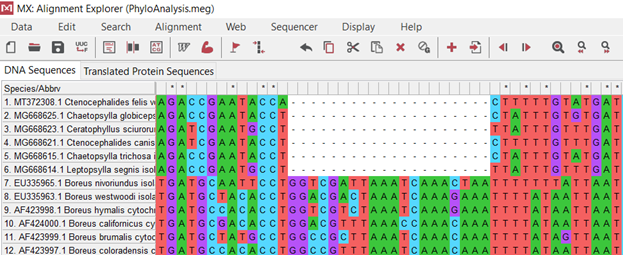
(.3.)
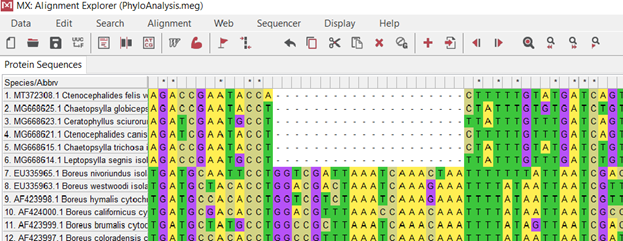
(.4.)
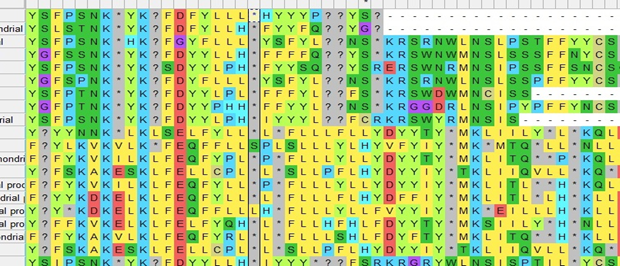
(.5)
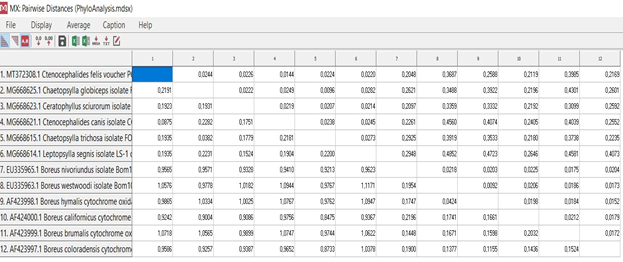
. Mecoptera Siphonaptera. 60% , Mecoptera Siphonaptera. , , , .
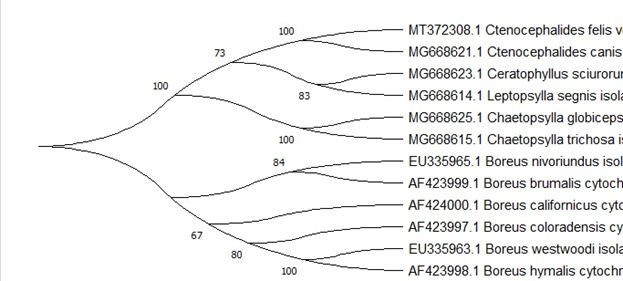
, MEGA X [4] (80%-100%) , . Ceratophyllus sciurorum Leptopsylla segnis (73%), . , (.. .2009; Whiting 2002; Whiting et al. 2008).
Mecoptera Siphonaptera . . Boreus nivoriundus Boreus brumalis (80%) «» Chaetopsylla globiceps Chaetopsylla trichosa (100%). , Mecoptera Siphonaptera. Boreus californicus (67%) . , . (.6.)
(.6.)
. . , , , . . . . [https://vk.com/phanerozoi] . , .
.
, , .
, .
1. Whiting M.F. 2002. Mecoptera is paraphyletic: multiple genes and phylogeny of Mecoptera and Siphonaptera. Zoologica Scripta, 31: 93–104
2. Whiting M.F., Whiting A.S., Hastriter M.W. and Dittmar K. 2008. A molecular phylogeny of fleas (Insecta: Siphonaptera) and host associations. Cladistics, 24: 1–31.
3. , .. , 313, № 3, 2009, c. 273–282
4. (SIPHONAPTERA) .., .. III , 2009, . 185-190
5. / .. —.. , 2009. — .256. .29-31.
6. Posada, D., Buckley, T.R., 2004. Model selection and model averaging in phylogenetics: advantages of the AIC and Bayesian approaches over likelihood ratio tests. Syst. Biol. 53, 793–808.
7. Posada, D., Crandall, K.C., 1999. Modeltest. Bioinformatics 14, 817–818.
1. http://lifemap.univ-lyon1.fr
2. Sneath P.H.A. and Sokal R.R. (1973). Numerical Taxonomy. Freeman, San Francisco.
3. Felsenstein J. (1985). Confidence limits on phylogenies: An approach using the bootstrap. Evolution 39:783-791
4. Kumar S., Stecher G., Li M., Knyaz C. et Tamura K. ( 2018 ). MEGA X: Analyse génétique évolutive moléculaire sur toutes les plates-formes informatiques. Biologie moléculaire et évolution 35 : 1547-1549.
5.https: //www.ncbi.nlm.nih.gov/pmc/articles/PMC4681159/
6. Tajima F. et Nei M. ( 1984 ). Estimation de la distance évolutive entre les séquences nucléotidiques. Biologie moléculaire et évolution 1 : 269-285.